

Era a França do séc. XVIII.
O rei era Luís XVI. A situação financeira da França era grave.
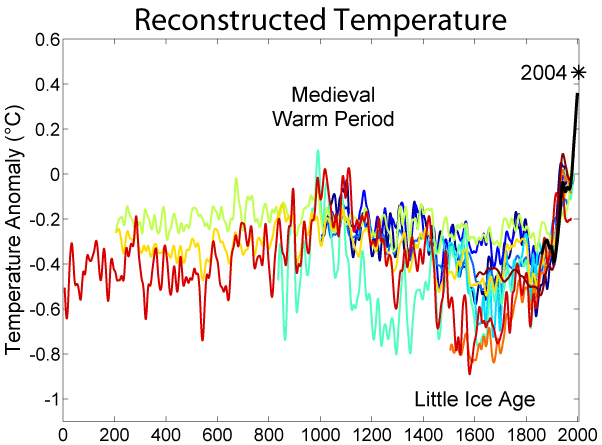
A Europa enfrentava um dos três períodos mais frios da Pequena Idade do Gelo.
O povo sofria um verdadeiro morticínio devido à fome. É famosa, deste período, a frase atribuída a Maria Antonieta: "Se não têm pão, que comam brioches".
O Período Medieval Temperado tinha causado um aumento populacional e de produção agrícola na Europa, com expansão de vinhedos e a instalação dos nórdicos na Groelândia. Ao contrário, neste mesmo período, parece ter havido grandes secas nas Américas, com registros de combates ferozes, subnutrição, redução dos deslocamentos comerciais, o colapso da cultura Maia e andina e do povo que habitava Angkor Wat, no Camboja.
No entanto, os sucessivos períodos de frio a seguir causaram grandes reduções na produção agrícola de alimentos. O frio foi tão intenso que acostumou-se a fazer uma feira em Londres sobre o rio Tâmisa congelado.

Este fato aparece no filme Orlando, quando ele, ainda homem, dança com a princesa russa Sasha.

Diz-se, mesmo, que o Rei Henrique VIII, certa vez, pode ir de Londres a Greenwich, distanciadas cerca de 10 km, em um trenó.
Galileu demonstrara a existência do vácuo e Boyle ressuscitara a teoria corpuscular da matéria.
Enquanto a Física, graças a Galileu e Newton, já integrava a Matemática, a Química permanecia no Mito, ainda com resquícios da Alquimia, envolvendo a noção de qualidades (cor, forma, etc.), a teoria dos quatro elementos, etc.
O trabalho dos químicos seguia a velha máxima alquimista da 14ª prancha do Mutus Liber de 1677:
"Ora, lege, lege lege relege labora et invenies" (Reza, lê, lê, lê, relê, trabalha e encontrarás).

No ensino de Química o professor ensinava a teoria e, depois, o assistente demonstrador 'comprovava' a verdade estabelecida pelo professor.

As substâncias, aos milhares, eram ensinadas uma a uma, apenas pelas suas propriedades físicas, mineralógicas, utilidades comerciais, etc. que os alunos tinham que decorar. Não haviam, ainda, sido classificadas em famílias, tais como óxidos, carbonatos, etc, como hoje.
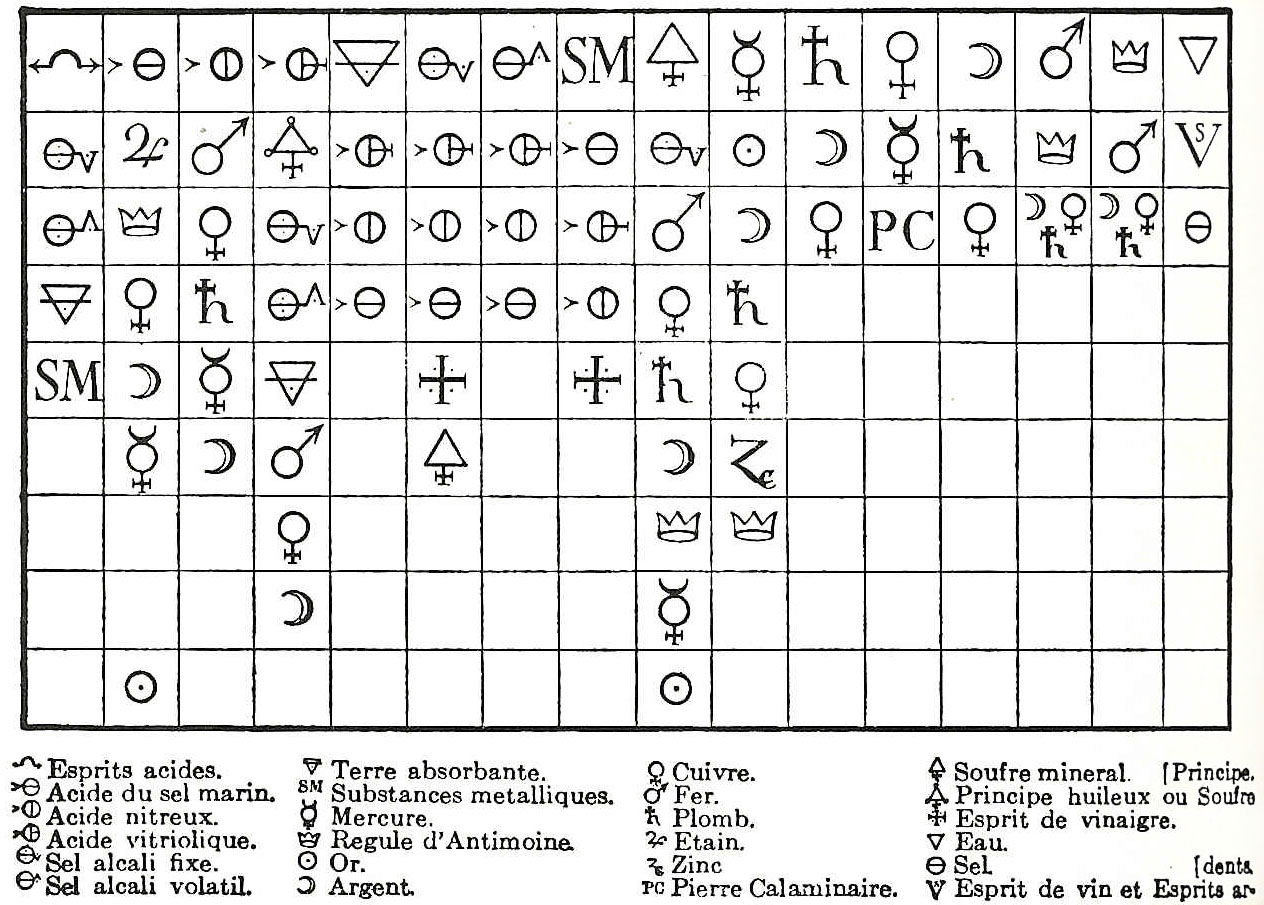
Pior, ainda eram usadas a simbologia e as denominações alquímicas, tal como nesta Tabela de Afinidades Químicas (1718), de Geoffroy.
 Lavoisier
nasceu em berço de ouro,
filho de uma família abastada, embora não
nobre.
Lavoisier
nasceu em berço de ouro,
filho de uma família abastada, embora não
nobre.Casou-se com Marie-Anne Pierette Paulze, jovem aristocrata de apenas 13 anos, casamento arranjado para resolver o problema de sua recusa em casar-se com o Conde de Amerval, um aristocrata falido de cinquenta e um anos, contornando a imposição de Joseph Marie Terray, membro superior da Ferme Général.
Marie-Anne interessou-se por Química, estudou e tornou-se valiosa parceira de Lavoisier, tendo traduzido para ele vários livros de Química em latim e em inglês. Também participou em várias experiências, como assistente, compilando dados, preparando relatórios e precisas e detalhadas ilustrações para suas obras.
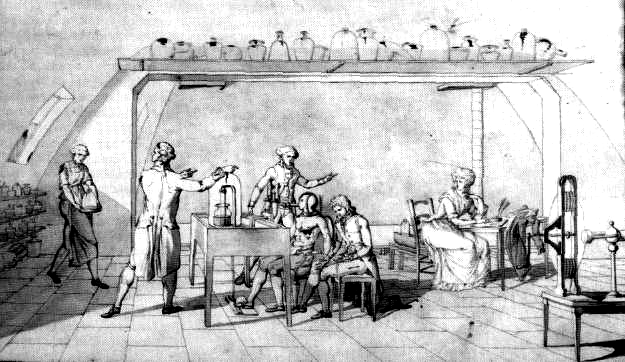
Como membro da Académie des Sciences, participava de comissões de investigação de novas teorias e/ou fenômenos, dando pareceres sobre sua legitimidade científica, tal como os pareceristas dos periódicos científicos de hoje.
Dentre essas investigações, concluíram pela inexistência do 'fluxo magnético animal', base do Mesmerismo.
Lavoisier tinha o sonho de "levar a mente ao laboratório", isto é, raciocinar de olhos abertos, pela manipulação de coisas reais ao invés de palavras e idéias vagas, como era o costume, até então.
Pregava um método analítico, baseado em experiências verificáveis e reprodutíveis, com instrumentos cada vez mais precisos e padronizados.
Através da introdução da balança, ele acrescentou precisão ao método experimental, já preconizado por Bacon, Galileu e Newton, realizando as primeiras experiências químicas realmente quantitavivas, inaugurando a Estequiometria e propondo as primeiras Leis químicas quantitativas.
Lavoisier também estudou calorimetria animal, tendo, juntamente com Laplace, desenvolvido um calorímetro de gelo
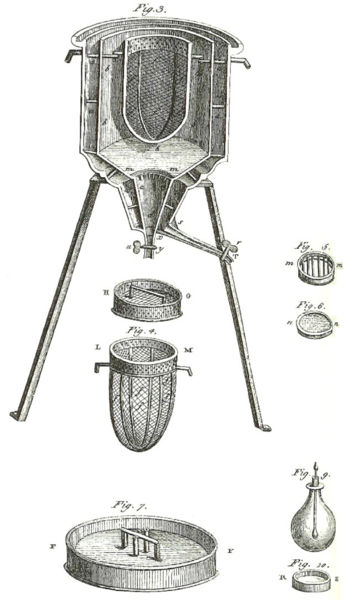
e introduzido o termo ‘caloria’, unidade de medida do calórico, como veremos adiante.
 Embora, como dissemos na aula As
Contribuições de Galileu e Newton, tivesse
sido, ele próprio, um alquimista, Boyle,
em sua obra magistral The Sceptical Chymist
(O Químico Cético), havia se
esforçado
em derrubar a concepção grega
dos quatro
elementos, e suas
interconversões, e a concepção
alquímica dos três princípios
(sal, mercúrio e
enxofre 'filosóficos', não os
comuns), demonstrando
que eles não são
verdadeiramente elementos, mas compostos.
Embora, como dissemos na aula As
Contribuições de Galileu e Newton, tivesse
sido, ele próprio, um alquimista, Boyle,
em sua obra magistral The Sceptical Chymist
(O Químico Cético), havia se
esforçado
em derrubar a concepção grega
dos quatro
elementos, e suas
interconversões, e a concepção
alquímica dos três princípios
(sal, mercúrio e
enxofre 'filosóficos', não os
comuns), demonstrando
que eles não são
verdadeiramente elementos, mas compostos. Apesar disso, até a época de Lavoisier, ambas concepções mantinham-se em força. Assim, por exemplo, a experiência de que a fervura prolongada da água (impura, como era) deixava um resíduo terroso, era tida como 'prova' da conversão do 'elemento' água no 'elemento' terra.
Coube a Lavoisier, utilizando a balança, demonstrar que a massa inicial da água era igual à massa da 'terra' restante somada à massa do vapor d'água.
Por um procedimento análogo, demoliu a crença de Boyle de que, durante uma calcinação, 'partículas de fogo' atravessariam a porosidade do vidro e se incorporariam ao metal, por forma a aumentar o peso da cinza resultante. Ao contrário, demonstrou que não havia variação de massa até que o vidro fosse aberto, quando, então, o oxigênio do ar se combinaria com o metal.
Com essas e outras experiências, Lavoisier foi capaz de enunciar, 14 anos após Lomonossov, a Lei da conservação da matéria, também conhecida como Lei da conservação das massas que, em forma popular, se expressa como
"Na Natureza nada se cria, nada se perde, tudo se transforma."
Um ponto importante, aqui, é que Lavoisier chegou a essa Lei, uma grande indução, diga-se, a partir de um procedimento empírico, quantitativo, e não por considerações racionalistas filosóficas, como até então tinha sido a Química!
Voltar à Parte Anterior
Voltar a Minhas Aulas.
Voltar ao começo desta página
Voltar à página principal de Física Interessante